ОРГАНИЧЕСКАЯ ХИМИЯ в томском государственном университете |
Методы очистки и выделения белков. Часть 2.
Перед тем, как определять первичную структуру белка, белок очищают от многочисленных примесей, среди которых присутствуют: другие белки, неорганические соединения, низкомолекулярные соединения и т.д. Наиболее опасными примесями в белках являются различные протеазы- ферменты, расщепляющие полипептидную цепь белка. Очистка белков осложняется также большей подверженности чистых белков денатурации. Все вместе взятое усложняет процесс получения чистого белка в количествах, обеспечивающих возможность определения первичной структуры.
Чистота полученного белка (так называемая гомогенность) должна быть подтверждена не менее, чем двумя методами, и еще лучше- иммуноблоттингом, который подтверждает наличие у материала антигенных детерминант, присущих нативному (натуральному, неповрежденному) белку.
Для разделения белков используют такие их физико-химические характеристики, как наличие зарядов, степень гидрофобности, молекулярная масса, наконец, специфические взаимодействия.
Электрофоретические методы разделения протеинов
Капиллярный электрофорез (CE, CE/MS)
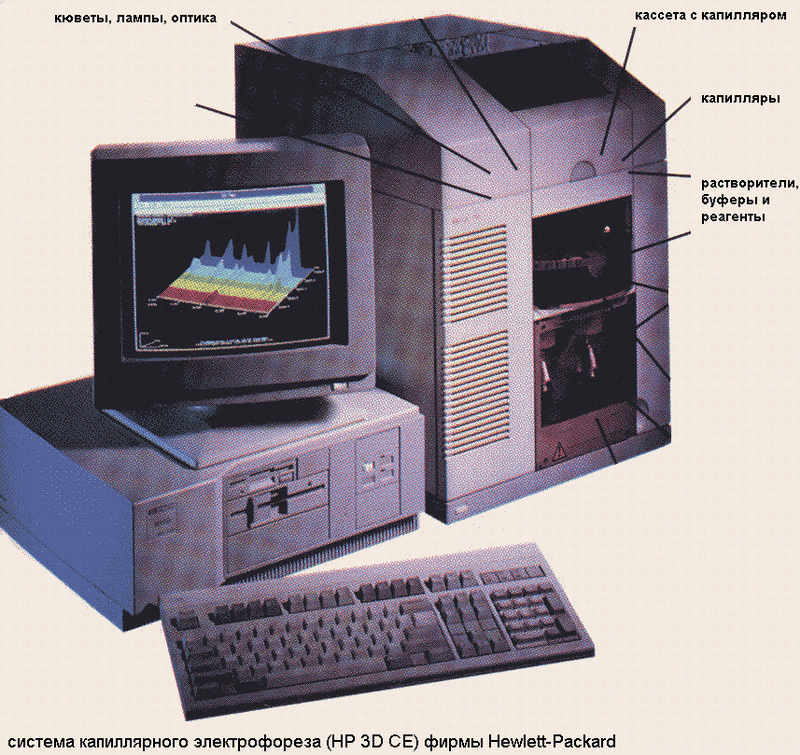
Выполняется на капиллярных колонках длиной от 40 см до 1 м. К концам пустотелого кварцевого которого прикладывается разность потенциалов в 10-30 кВ. Под действием электрического поля начинается движение ионов (+) электролита, уравновешивающих отрицательно заряженные группировки ионизированных силанольных групп на внутренней поверхности кварцевого капилляра. Двигающиеся ионы увлекают за собой молекулы растворителя, что вызывает общее течение жидкости в капилляре. Явление носит название электроосмотический поток (ЭОП, EOF). При введении в такую систему анализируемого образца положительно заряженные молекулы анализируемых соединений движутся к катоду быстрее потока жидкости в капилляре, незаряженные молекулы «текут» с потоком, а отрицательно заряженные, удерживаясь положительным зарядом, текут медленней всего, но тем не менее, текут к катоду. Происходит весьма эффективное разделение молекул по зарядам. Этот вариант электрофореза в капилляре наиболее прост и называется зонным электрофорезом (CZE, или КЗЭ). Идентификация осуществляется спектрально (прямая или косвенная УФ-индикация) или другим подходящим способом (часто- масс-спетрометрически-CE/MS).
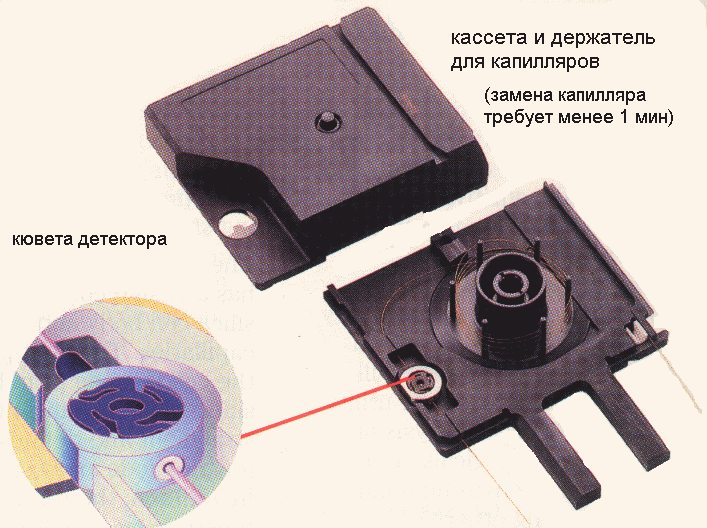
Среда разделения.
Используются пустотелые кварцевые капилляры внутренними диаметрами 50, 75 и 100 мкм и с эффективной длиной 24,5, 40, 56, 72 и 104 см. С наружной стороны капилляры имеют полиамидное покрытие, улучшающее их прочность. Торцы капиляров обработаны с зеркальной чистотой поверхности. Предусмотрено "окошко" для детектирования по УФ. Кроме того, имеются капилляры с удлиненным оптическим путем детектирования (для капилляров с внутренним диаметром 25 мкм оптический путь составляет 125 мкм, для 50-мкм капилляров- 150 мкм, а для 75 микронных- 200 мкм).
Покрытые изнутри поливиниловым спиртом (PVA-coated) капилляры минимизируют гидрофобные и электростатические взаимодействия анализируемых соединений со стенками и, кроме того, снижают электроосмотический поток. Покрытие стабильно в растворах с рН от 2,5 до 9,5. Все это улучшает форму пиков и воспроизводимость времен удерживания.
Капилляры для капиллярной электрохроматографии (СЕС). Имея внутренний диаметр 100 мкм, капилляры заполнены сорбентом для ВЭЖХ (силикагелевые частицы размером 3 мкм с привитой фазой) под наименованием CEC-Hypersil. В качестве привитой фазы применены углеводородные цепи С8, С18 и Фенил. Капиллярная электрохроматография сочетает разделительную способность ВЭЖХ и эффективность капиллрного электрофореза. На обоих концах капилляров можно создавать избыточное давление для предотвращения выделения пузырьков газа в результате наложения высокого потенциала. Существуют капилляры, заполненные сорбентами с различными диаметрами пор для гель-проникающей хроматографии (разделения молекул по размерам).
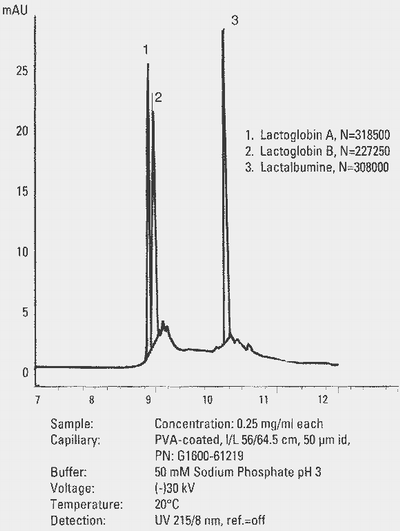
Капиллярный электрофорез отличается от родственных ему методов жидкостной хроматографии чрезвычайно высокой эффективностью разделения, теоретическое объяснение которой не найдено до сих пор. Типичный пример разделения белков капиллярным электрофорезом (указано число т.т. по пику каждого соединения):
Расписание занятий преподавателей кафедры органической химии
© khassanov @ MMII - MMXVIII |