
Лекция № 3. Ароматические соединения.
Ароматическими называются ненасыщенные циклические системы из атомов углерода (иногда с включениями вместо одного или нескольких атомов углерода гетероатома (N, O, S)), по которым возможна делокализация определенного числа электронов.
Итак, ароматической называется система, отвечающая всем перечисленным ниже условиям:
Ниже приведены примеры ароматических систем:
Типичной ароматической системой является бензол и его гомологи. Вследствие наличия делокализации электронов по кольцу внутренняя энергия ароматической системы является пониженной, а структура в целом является более устойчивой. Разница в теплоте сгорания бензола и теоретически рассчитанной теплоте сгорания гипотетического циклогексатриена составляет энергию стабилизации. Она для бензола примерно равна 36 ккал/моль. Энергия стабилизации получается как разница между расчетной и экспериментальной теплотами гидрирования:

Циклогксадиен-1,3 обладает небольшой энергией стабилизции в 2,3 ккал/м, вследствие сопряжения двух кратных связей. Но она не идет ни в какое сравнение с энергией стабилизации бензола вследствие его ароматичности.
Номенклатура ароматических соединений.
Наиболее распространенными ароматическими углеводородами являются бензол и его гомологи, а также полиядерные ароматические соединения: нафталин, антрацен, фенантрен, тетрацен, пентацен и т.д.

Номенклатура замещенных бензолов
При наличии в кольце двух заместителей, они могут располагаться в нем тремя различными способами:

При наличии в кольце трех и более заместителей удобней пользоваться номенклатурой ИЮПАК:

Порядок нумерации атомов углерода кольца
определяется таким образом, чтобы сумма номеров заместителей оказалась наименьшей.
Если название образуется от наименования гомолога или производного бензола (толуол,
фенол и т.д.), тогда первый номер присваивается группировке, определяющей название
(СН3- для толуола, НО- для фенола), а направление нумерации выбирают так, чтобы
получить минимальную сумму номеров заместителей:

Химические свойства ароматических соединений.
Ароматическая система стремится сохранить свою стабильность даже в результате химических превращений. Отсюда появляется особая устойчивость ароматических систем, роднящая их с алканами. Несмотря на наличие существенной степени ненасыщенности, ароматические соединения не вступают в реакции присоединения, характерные для алкенов и алкинов (за очень редкими исключениями). Таким исключением является присоединение 6 атомов хлора к бензолу на свету с образованием неароматического гексахлорциклогексана (ГХЦГ):

Более характерными реакциями для ароматики являются реакции замещения. В отличие от алканов, реакции замещения в ароматических системах могут протекать как по радикальному, так и по ионным механизмам. Более того, условия реакции (и наличие или отсутствие катализатора) определяют направление реакции- по боковому радикалу или реакция с замещением в кольце. Реакции радикального замещения по алкильным заместителям ароматического кольца протекают по тому же радикальному механизму, что и реакции замещения в алканах:
Реакции замещения в кольцо протекают только через образование положительно заряженных промежуточных частиц. В частности, к таким относят реакции электрофильного замещения, протекающие по общему механизму: Замещаемой частицей является протон.
По такому механизму протекают реакции алкилирования, галогенирования, сульфирования, нитрования ароматических соединений и другие, различаясь лишь способом образования активной частицы реакции- электрофила Е+: а) нитрование: HO-NO2 + H2SO4 -->
H2O + NO2+ + HSO4- б) сульфирование: HO-SO3H + H-SO4H -->
HSO3+ + HSO4- в) галогенирование Cl2 + AlCl3 -->
Cl+ + AlCl4- г) алкилирование: CH3-CH2-Cl + AlCl3 -->
CH3-CH2+ + AlCl4-
В незамещенном кольце бензола все 6 положений равноценны для вхождения замещающей
группы. Сложнее обстоит дело, если в реацию вступают гомологи или производные
бензола. В этом случае вновь входящая группа вступает в определенное место в
кольце. Это место зависит от уже имеющегося (или имеющихся) в кольце заместителя.
Например, если в кольце имеется электронодонорная группировка типа: Алкил-,
-ОН,
-ОСН3,
-NH2, -NHR, NR2, -NH-COR, -Х
(галоген) (заместители
первого рода), то замещающая группа
вступает в орто- или пара- положения относительно имеющейся группы: Если в кольце уже имеется электроноакцепторная группировка типа: -NO2, -NO, -SO3H, -CX3, -COOH, -COH, -COR, -CN (заместители второго рода), то вновь вступающая группа становится в мета- положение к ним: Если в кольце имеется два заместителя разного рода, направляющие замещение несогласованно, то место вступления новой группы определяется по заместителю первого рода, например:
В данном случае наблюдается согласованная
ориентация. Другие химические реакции ароматических
соединений. Окисление Ароматические соединения способны окисляться кислородом воздуха в присутствии ванадиевоокисного катализатора с разрушением ароматического кольца: Алкилзамещенные гомологи бензола окисляются при кипячении в растворе KMnO4 до соответствующих карбоновых кислот. Строение алкильной группы при этом значения не имеет: Методы получения бензола и его гомологов Основным источником ароматических соединений является нефть.
Различные сорта нефти существенно различаются содержанием ароматических углеводородов.
Другим важным источником ароматических соединений является каменноугольная смола,
получаемая в процессе производства кокса для целей металлургии. 2. Ацетон при действии концентрированной серной кислоты образует 1,3,5-триметилбензол
(мезитилен). Реакция представляет собой случай циклической кротоновой конденсации
трех молекул кетонов. Подобным образом ведут себя все метилкетоны. 3. Реакцией ароматизации алканов с числом атомов углерода не менее 6. Н. Д. Зелинский, Б. А. Казанский и А. Ф. Платэ в 1912 году получили бензол из гексана, метилбензол из гептана и
гомологи бензола из других алканов , пропуская их пары над платиной или палладием при 300 С, попутно получается водород. 4. Важным способом лабораторного получения гомологов бензола является алкилирование
ароматических углеводородов по способу Фриделя-Крафтса, открытому в 1877 г.
(см. свойства ароматических углеводородов выше). Однако, этим способом могут
быть получены только алкилбензолы с разветвленными углеводородными радикалами. 5. Гомологи бензола с нормальными углеводородными цепями получают ацилированием бензола и его гомологов по Фриделю-Крафтсу и последующим восстановлением полученных
фенилкетонов:
Небензоидные
ароматические системы © khassanov, MMII-MMXVII 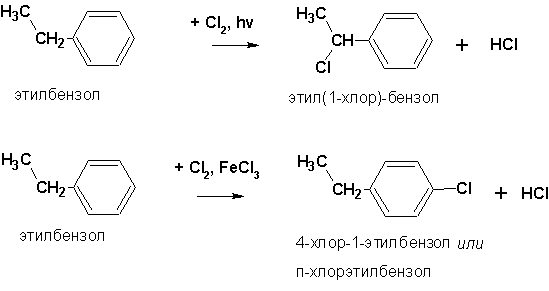







Из синтетических способов получения бензола и его гомологов следует указать:
1. В 1912 г. Н. Д. Зелинский осуществил ароматизацию циклогексана над платиновым
катализатором и получил бензол. Он же в сотрудничестве с Б. А. Казанским в 1922
году получил бензол из ацетилена, пропуская последний через активированный древесный
уголь при 450-500 С.
Позднее аналогичные превращения были осуществлены нагреванием алканов с серой
при 400 С или селеном при 500 С. Водород в этих случаях выделяется в виде сероводорода
или селеноводорода.
